肿瘤炎症微环境调控肝癌转移复发新机制
【字体: 大 中 小 】 时间:2017年02月14日 来源:吉凯基因
编辑推荐:
2016年6月,国际消化病顶级杂志《Gastroenterology》(胃肠病学,IF=18.2)以长文(Original Research)形式正式发表了复旦大学(附属中山医院)肝癌研究所周俭教授研究团队的肿瘤炎症微环境调控肝癌转移复发最新研究成果。
炎症被认为是肿瘤的第七大特征,肿瘤相关性炎症和肿瘤的发生,发展密切相关。原发性肝癌是全球发病率和死亡率均较高的恶性肿瘤之一,一般经历肝炎-肝硬化发展而来,深入研究肝癌相关的炎症微环境对于肝癌的诊疗及预测预后有极大的价值。
2016年6月,国际消化病顶级杂志《Gastroenterology》(胃肠病学,IF=18.2)以长文(Original Research)形式正式发表了复旦大学(附属中山医院)肝癌研究所周俭教授研究团队的肿瘤炎症微环境调控肝癌转移复发最新研究成果"Tumor-Associated Neutrophils Recruit Macrophages and Treg Cells to Facilitate Hepatocellular Carcinoma Progression and Resistance to Sorafenib ",首次揭示中性粒细胞作为肿瘤微环境中的一个重要炎症细胞,通过招募巨噬细胞和调节性T细胞(Treg)浸润,参与调控肿瘤的侵袭与转移。
肿瘤的侵袭和转移是肿瘤细胞、宿主和肿瘤微环境之间一系列复杂、多步骤、多因素相互作用的序贯连续过程。肿瘤微环境中肿瘤细胞与不同免疫/炎症细胞-细胞、细胞-间质间的相互作用对肝癌转移复发具有重要影响。其中肿瘤相关性中性粒细胞(tumor-associated neutrophils, TANs) 是指肿瘤微环境中浸润的中性粒细胞,形态上为成熟粒细胞,表达中性粒细胞的表面标志。周俭教授课题组前期报道肝癌细胞通过分泌趋化因子CXCL5介导中性粒细胞浸润,促进肝癌转移复发,相关结果已发表于国际肝脏病权威杂志Hepatology(IF=11.7)。课题组在肝癌细胞株和小鼠移植模型中深入研究发现肝癌中TANs高丰度分泌细胞因子CCL2招募巨噬细胞,同时分泌CCL17介导Treg浸润,三者共同促进肿瘤生长、血管生成以及侵袭转移(图一左)。此外,体外细胞共培养实验表明肝癌细胞通过激活正常中性粒细胞的PI3K/Akt 和 p38/MAPK信号通路,使其"驯化"为TANs,进而分泌细胞因子CCL2 和 CCL17(图一左)。值得注意的是,研究者发现索拉菲尼治疗引起缺氧,诱导肝癌细胞通过HIF1α/NF-κB/CXCL5通路招募中性粒细胞浸润(病毒载体购于吉凯基因),同时抑制其凋亡,因此制约了索拉菲尼的疗效(图一右和图二)。体内成瘤实验中,研究人员证实封闭中性粒细胞联合索拉菲尼治疗显示出协同抑制肿瘤生长和血管生成作用。该成果以肝癌为研究对象,系统的研究了肝癌微环境中炎症/免疫细胞之间的相互调控及其在肝癌转移复发中的作用与机制,深入探讨了以间质细胞作为潜在肿瘤分子靶点的可行性。
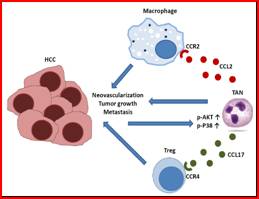
图一:左:TANs招募巨噬细胞和调节性T细胞(Treg)浸润
右:肝癌细胞招募中性粒细胞浸润,并抑制其凋亡。
图二:利用吉凯基因包装的干扰病毒证明肝癌细胞通过HIF1α/NF-κB/CXCL5通路招募中性粒细胞浸润。
作者介绍:周少来博士,复旦大学附属中山医院肝肿瘤外科住院医师,主要从事肝癌炎症微环境调控肿瘤侵袭转移的机制研究,近五年以第一作者在Gastroenterology 、Hepatology等杂志正式发表SCI论著10篇,累积影响因子79.8,他引200余次。目前作为课题负责人主持国家自然科学基金青年基金和上海市扬帆计划课题各1项。
原文转自:吉凯基因微信公众号